いのちの現場
2026/02/25
CiRA長船先生インタビュー【前編】 iPS細胞による創薬・再生医療の現在地
- メディカル事業
- バイオ
- 技術開発

目次
2012年に山中伸弥教授がノーベル生理学・医学賞を受賞し、世界的な注目を集めたiPS細胞。体のあらゆる細胞になれる多能性を持ち、再生医療や創薬研究に革命をもたらした技術は今、どこまで実用化が進んでいるのでしょうか?
今回は、京都大学iPS細胞研究所「Center for iPS Cell Research and Applicaition(CiRA; サイラ)」副所長・長船健二先生にインタビュー。前編となる本記事では、iPS細胞の基礎知識から、iPS細胞による再生医療や創薬の最前線まで、分かりやすく教えていただきます。
| 長船 健二 京都大学iPS細胞研究所(CiRA)副所長・教授。 1996年京都大学医学部卒業。一般内科、腎臓内科、透析医学の臨床経験を積んだ後、東京大学大学院で腎臓の発生・再生医学を研究し博士号取得。ハーバード大学幹細胞研究所を経て2008年にCiRAの前身組織の立ち上げメンバーとして京都大学へ戻り、2014年より教授、2024年より副所長を務める。現在はiPS細胞を用いた腎臓・膵臓・肝臓の再生医療および創薬を中心に研究を進めている。 |
iPS細胞研究の現在地
――まず、長船先生が所属しているiPS細胞研究所(CiRA)の役割を教えてください。
長船先生: CiRAは、山中伸弥先生が2006年にマウスで、2007年にヒトでiPS細胞を樹立されたことを受け、その技術を医療に応用することを使命として2010年に設立されました。現在、約600名の教職員と学生が在籍し、基礎研究だけでなく、患者さんに届けるための「医療応用」の研究を進めています。
 京都大学吉田キャンパス内に拠点を置くiPS細胞研究所(CiRA)
京都大学吉田キャンパス内に拠点を置くiPS細胞研究所(CiRA)
 CiRAオープンラボの様子
CiRAオープンラボの様子
――改めて、iPS細胞の特徴について教えてください。
長船先生:iPS細胞には2つの大きな特徴があります。まず「無限に増えること」、そして「体のあらゆる細胞になれること」です。私たちの体は約200種類の細胞からできていますが、理論上そのすべてを作り出すことができます。
当初は皮膚の細胞を使って作製していましたが、研究が進み、どんな細胞からでもiPS細胞を作れるようになりました。現在では血液の細胞から作製することが多く、採血のみで済むため、患者さんの負担も少なくなっています。
――iPS細胞はどのように作製されるのでしょうか?
長船先生:採取した血液の細胞に特定の初期化因子を導入することで、iPS細胞を作製できます。山中先生が最初に開発したのは、「山中4因子」と名付けられた4つの特定の遺伝子を、レトロウイルスベクター(※1)を用いて細胞の核内の染色体に組み込む方法でした。
しかし、この手法では染色体内のどこに遺伝子が組み込まれるかコントロールできず、染色体が傷つき、将来的にがん化するリスクが懸念されていました。がん化しないiPS細胞を目指し、CiRAでさらなる研究を行った結果、ベクターや因子を変え、染色体を傷つけない安全な作製法を確立しました。
現在、日本で行われている臨床研究では、この安全な方法で作られたiPS細胞が使用されており、がん化のリスクは極めて低くなっています。実際、この10年以上の再生医療の試験において、iPS細胞由来の細胞ががん化したという報告は一例もありません。また、近年mRNA(※2)などを用いた作製方法も開発されており、今後はそちらが主流になっていくと考えられています。
(※1)レトロウイルスベクター:遺伝子運搬役(ベクター)で、目的の遺伝子を細胞の核内の染色体に組み込み、長期的に安定して発現させることができる。一方で、染色体内の挿入部位がランダムで、がん関連遺伝子を傷つけて活性化するリスクがある。
(※2)mRNA:細胞の遺伝情報を写し取り、タンパク質をつくる指令を伝える物質。
――iPS細胞が開発された当時、自分だけのiPS細胞で治療が受けられるようになる、と期待されていました。現在はどのような状況でしょうか?
長船先生: まず、人間には体内の異物を排除する免疫機能が備わっています。他人の臓器や細胞を移植すると、この免疫機能が移植した細胞を異物と判定し攻撃を始めます。そのため、臓器移植を行うときは、通常免疫抑制剤が必要となるのです。しかし、免疫抑制剤には免疫力の低下による感染症への罹患リスクや、長期的な使用による発がんリスクもあります。
iPS細胞の最大の良い点は、患者さんご自身の細胞から作れば拒絶反応のない移植ができ、この免疫抑制剤が不要となることです。しかし、自家移植には「時間」と「お金」という大きな問題があります。患者さんの血液からiPS細胞を作ることは1か月程度でできますが、同じ血液からiPS細胞を同じ条件で作っても、性質の異なる多くのクローンが出来上がります。その中から最適な細胞を選ぶのに1年はかかりますし、移植できるまで細胞を分化させるには、さらに数か月を要します。また、現状では数千万円規模の費用もかかります。
そこでCiRAが進めてきたのが「iPS細胞ストックプロジェクト」(※3)です。これは、拒絶反応が起きにくい特殊な遺伝子の型(HLAホモ)を持つ健康なドナーの方からあらかじめiPS細胞を作製し、品質評価を行った上で備蓄(ストック)しておくものです。これならば、必要なときにすぐ、比較的安価に細胞を提供できます。
もちろん、自分自身のiPS細胞を作れる仕組みも出てきつつあります。しかし、まだ開発途中のため、それらを治療に使えるようになるまでにはまだ時間がかかるでしょう。そのため、現時点で多くの患者さんを救うためには、ストックを利用した方法が現実的であり、研究の中心となっています。
(※3)本プロジェクトは、現在、公益財団法人京都大学iPS細胞研究財団に引き継がれています。 再生医療用iPS細胞の製造・品質試験を実施する細胞調整施設(FiT)
再生医療用iPS細胞の製造・品質試験を実施する細胞調整施設(FiT)
左:アイソレーター/中央:細胞保存タンク/右:培地交換の様子
(提供:京都大学iPS細胞研究所)
再生医療は安全性から「有効性」の確認へ
――iPS細胞を医療に応用する研究には、どのようなものがあるのでしょうか?
長船先生:大きく分けて2つのアプローチがあります。1つは「再生医療」です。これは病気や怪我で失われた細胞や組織を、iPS細胞から作製して移植し、機能を回復させる治療法です。これまで薬で症状を抑えることしかできなかった病気でも、細胞を補充することで根本的に治せる可能性があります。
もう1つは「薬の開発(創薬)」です。こちらは、iPS細胞を使って病気の状態の細胞を再現することで、新しい治療薬を見つけるというものです。
――まず、「再生医療」について、研究の進捗や成果を教えてください。
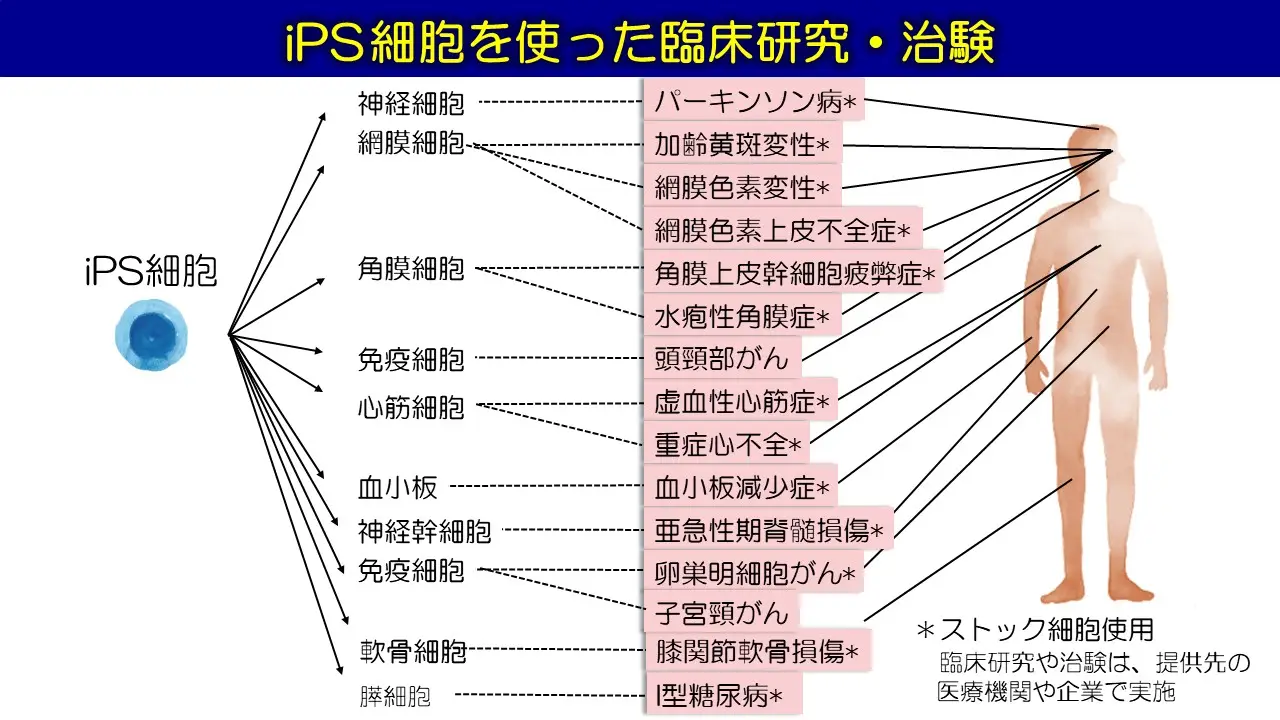
長船先生: 2014年に理化学研究所などが実施した「加齢黄斑変性症」に対する網膜色素上皮細胞の移植を皮切りに、この10年間でiPS細胞を使った再生医療は大きく進展しました。現在、日本国内だけでもパーキンソン病、難治性心不全、脊髄損傷、角膜疾患、膝関節軟骨損傷、がん免疫療法、血小板減少症など、10以上の疾患に対してiPS細胞を用いた細胞移植の臨床研究や治験が行われています。
 日本で行われているiPS細胞を使った再生医療の臨床研究・治験
日本で行われているiPS細胞を使った再生医療の臨床研究・治験
(提供:京都大学iPS細胞研究所)
特筆すべきは、これらの研究ですでに安全性だけでなく、治療の有効性を示唆する結果が出始めていることです。
たとえば、CiRAと京都大学病院が実施したパーキンソン病の治験では、iPS細胞から作った神経細胞を脳に移植し、有効性を調べた6名の患者さんのうち、4名で症状の改善が見られ、重篤な副作用も確認されていません。治療法に対する懸念の段階を越え、「治せなかった病気を治す」新しい医療として、患者さんの手元に届く日が近づいていると実感しています。
――次世代のiPS細胞も開発されていると伺いました。
長船先生: はい。先ほどの説明のとおり、他人の細胞を移植する場合、免疫抑制剤がどうしても必要になりますが、できるだけ使用を減らしたいのが本音です。
そこで現在、拒絶反応に関わるHLAなどの遺伝子を改変した「低抗原性iPS細胞」の開発が進んでいます。これにより、免疫抑制剤をほとんど使わずに移植できる次世代の治療法が期待されています。
既存薬から難病の治療薬を見つけ出す創薬研究
――iPS細胞のもう一つの柱である「創薬研究」について教えてください。
長船先生: 脳や心臓の病気は、患部から細胞を採取して研究することが難しいのですが、患者さんの血液からiPS細胞を作り、それを患部の細胞(神経や心筋など)に分化させることで、体の中で起きている病気の状態(病態)を再現できることが分かっています。これにより、試験管の中で治療薬の候補となる化合物を病態細胞に簡単に試すことができるようになりました。病気の進行を抑える薬を効率的に探すのがiPS細胞を用いた創薬です。
――具体的にどのような成果が出ていますか?
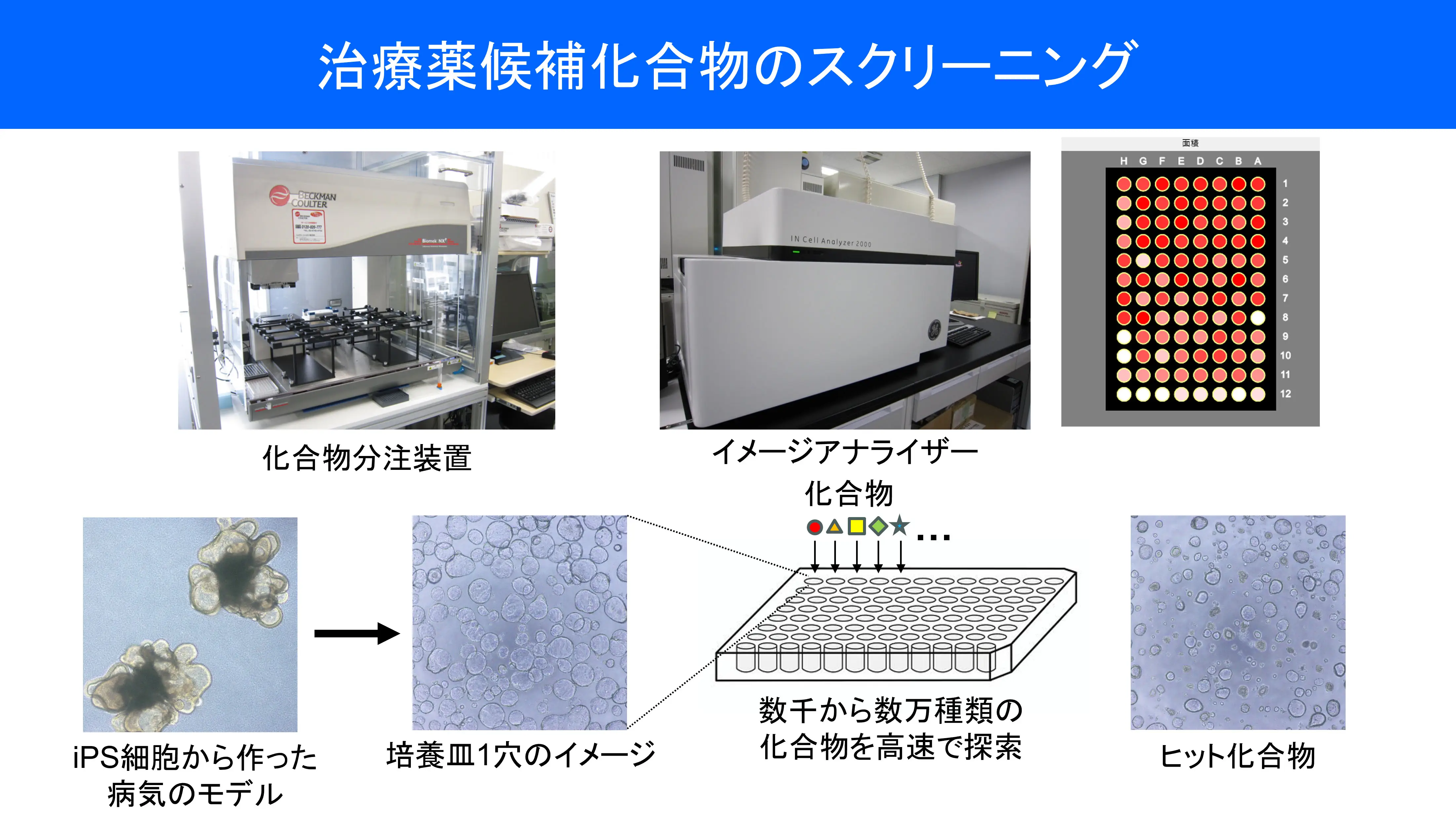
長船先生: 代表的な例として、ALS(筋萎縮性側索硬化症)の研究があります。患者さん由来のiPS細胞から作った神経細胞を用いて、数千種類の既存薬ライブラリーの中から効果がある薬を探す「ドラッグ・リポジショニング」という手法がCiRAの井上治久教授のグループによって行われました。これはすでに他の病気で使われていて安全性が確認されている薬から、別の難病への効果を見つけ出す手法で、ゼロから新薬を作るよりも開発期間を大幅に短縮でき、いち早く患者さんに治療を届けることができます。
このようにして、従来は白血病の治療薬として知られていた「ボスチニブ」が、ALSの神経細胞死を抑えることが発見されました。現在、この薬はALS患者さんを対象とした治験の最終段階に進んでいます。
 化合物スクリーニングの流れ。数千から数万種類の化合物を高速で探索できる。
化合物スクリーニングの流れ。数千から数万種類の化合物を高速で探索できる。
医療応用に向けたさらなる取り組み
――CiRAでの研究成果を社会実装するために、先生はどのような取り組みをされているのでしょうか?
長船先生:新しい治療法や薬は、実用化までの道のりが長く、どうしても初期段階では企業が参入しにくいのが現状です。そこで、フェーズ1、フェーズ2の臨床試験までの開発初期段階を自ら担い、企業に受け入れてもらいやすくしてはどうかと考えました。そうして私たちが2019年に設立したのが、「リジェネフロ株式会社」というバイオベンチャーです。
リジェネフロの使命は、研究の先にある「患者さんを救うこと」です。創設の背景には腎臓や膵臓、肝臓の細胞療法、そして難病の治療薬を一日でも早く実用化したいという強い想いがあります。
腎臓や膵臓、肝臓の疾患は患者数が多く、また、移植以外の根本的な治療法が少ないため、社会的意義の非常に大きい分野です。日機装をはじめとするパートナー企業の皆さまと共に、安全性と確実性を最優先に、一歩ずつ着実に実用化へ向けた取り組みを進めています。
後編では、リジェネフロの具体的な活動をご紹介します。
<iPS細胞研究基金について>
これまでにiPS細胞研究は大きく発展してきましたが、医療として確立されるまでにはまだまだ時間がかかります。この長い道のりを走り続けるための財源として、多くの方々からのご寄付で成り立っている「iPS細胞研究基金」は、研究活動を支える重要な柱となっています。
今は不可能な治療を一日も早く可能にするために、iPS細胞研究基金へのご支援をお願いいたします。
iPS細胞研究基金へのご支援についてはこちら。







