いのちの現場
2026/03/04
CiRA長船先生インタビュー【後編】 iPS細胞で腎臓を「治す」ために~リジェネフロと日機装が拓く再生医療の未来~
- メディカル事業
- バイオ
- 技術開発
- 金沢

目次
京都大学iPS細胞研究所(CiRA)の副所長であり、バイオベンチャー「リジェネフロ株式会社」の創設者でもある長船健二先生へのインタビュー特集。前編では、iPS細胞を用いた創薬・再生医療の現在地について伺いました。
後編となる本記事では、長船先生が腎臓内科医として抱き続ける原点と、リジェネフロが目指すiPS細胞の医療応用への道筋、そして、「細胞の大量培養」に挑む日機装との共同研究に迫ります。
| 長船 健二 京都大学iPS細胞研究所(CiRA)副所長・教授。 1996年京都大学医学部卒業。一般内科、腎臓内科、透析医学の臨床経験を積んだ後、東京大学大学院で腎臓の発生・再生医学を研究し博士号取得。ハーバード大学幹細胞研究所を経て2008年にCiRAの前身組織の立ち上げメンバーとして京都大学へ戻り、2014年より教授、2024年より副所長を務める。現在はiPS細胞を用いた腎臓・膵臓・肝臓の再生医療および創薬を中心に研究を進めている。 神保 陽一 日機装株式会社 メディカル事業本部 バイオ事業推進部 部長。 |
「治せない疾患」を無くしたい。「リジェネフロ」創設の原体験
――長船先生は25年以上にわたり、腎臓を研究されてきました。そのきっかけは何だったのでしょうか?
長船先生:医師になった1996年当時から、私は将来的に研究を行うことを見据えていました。
その中で純粋に興味を持ったのが、「なぜ臓器によって再生能力に差があるのか」ということでした。皮膚や血液は傷ついても盛んに細胞分裂して再生しますが、腎臓や神経は一度壊れると再生せず、機能が失われていく一方です。
当時、腎臓内科は今ほど確立されておらず、多くの病院では循環器内科の一部という扱いでした。しかし、高齢化に伴い腎臓病の患者さんが増えることは明らかであり、社会的に重要になる領域でありながら、根本的な治療法は深刻なドナー不足が問題となっている「腎移植」しかない。「なぜ再生しないのか」「どうにかして治せないか」という思いから、この研究分野を選びました。
――先生は、1日でも早く研究の成果を実用化したいという思いから、リジェネフロを創設されました。そこには学術的な研究の枠を超えた情熱を感じます。何か原体験があるのでしょうか?
 長船先生
長船先生
長船先生:私は本格的に研究を開始する前に、患者さんがどこで苦しんでいるのかを知るべきだと考え、研修医・臨床医として4年間現場に立ちました。
さまざまな経験をしましたが、そのなかでもとくに記憶に残っているのが、研修医時代に担当した遺伝性の腎臓病、ADPKD(常染色体顕性多発性嚢胞腎)を患う女性患者さんです。今でも、この病気に対する根本的な治療法はありません。透析、人工呼吸器、当時できる限りの手を尽くしましたが、彼女は30代という若さで亡くなりました。そのときの申し訳なさと治療法が無い歯痒さは、今でも鮮明に残っています。
他の診療科であれば、治療によって「良くなりましたね」と患者さんに言える場面があります。しかし、腎臓病の治療では、一度失われた機能は戻りません。「悪くなっていませんね」というのが精一杯。「良くなる方法がない」という現状を打破したいという一心で、2000年から本格的に研究を開始し、2019年にリジェネフロを創設しました。
基礎研究から臨床へ。創薬・腎臓再生で難病に挑む
――まず、「リジェネフロ」が目指すもの、現在の主な研究内容について教えてください。
長船先生:リジェネフロは、京都大学iPS細胞研究所(CiRA)での研究の成果を、実際の医療として患者さんに届けるために設立したバイオベンチャーです。私たちは基礎研究だけではなく、その先の実用化・臨床応用を最大のミッションとしています。
現在、大きく2つの研究開発を進めています。一つは、私の原点にもつながる、ADPKD(常染色体顕性多発性嚢胞腎)に対する創薬研究です。こちらはすでに候補となる薬を見つけ出し、約2年前から実際に患者さんに投与する臨床試験の段階に入っています。
そしてもう一つが、今回日機装と取り組んでいる「iPS細胞を用いた腎臓再生医療(細胞療法)」です。こちらは、腎臓の元となる細胞を移植することで、腎機能の低下を食い止めることを目指しており、2年後の臨床試験開始を目標に準備を進めています。
リジェネフロの事業詳細はこちら。
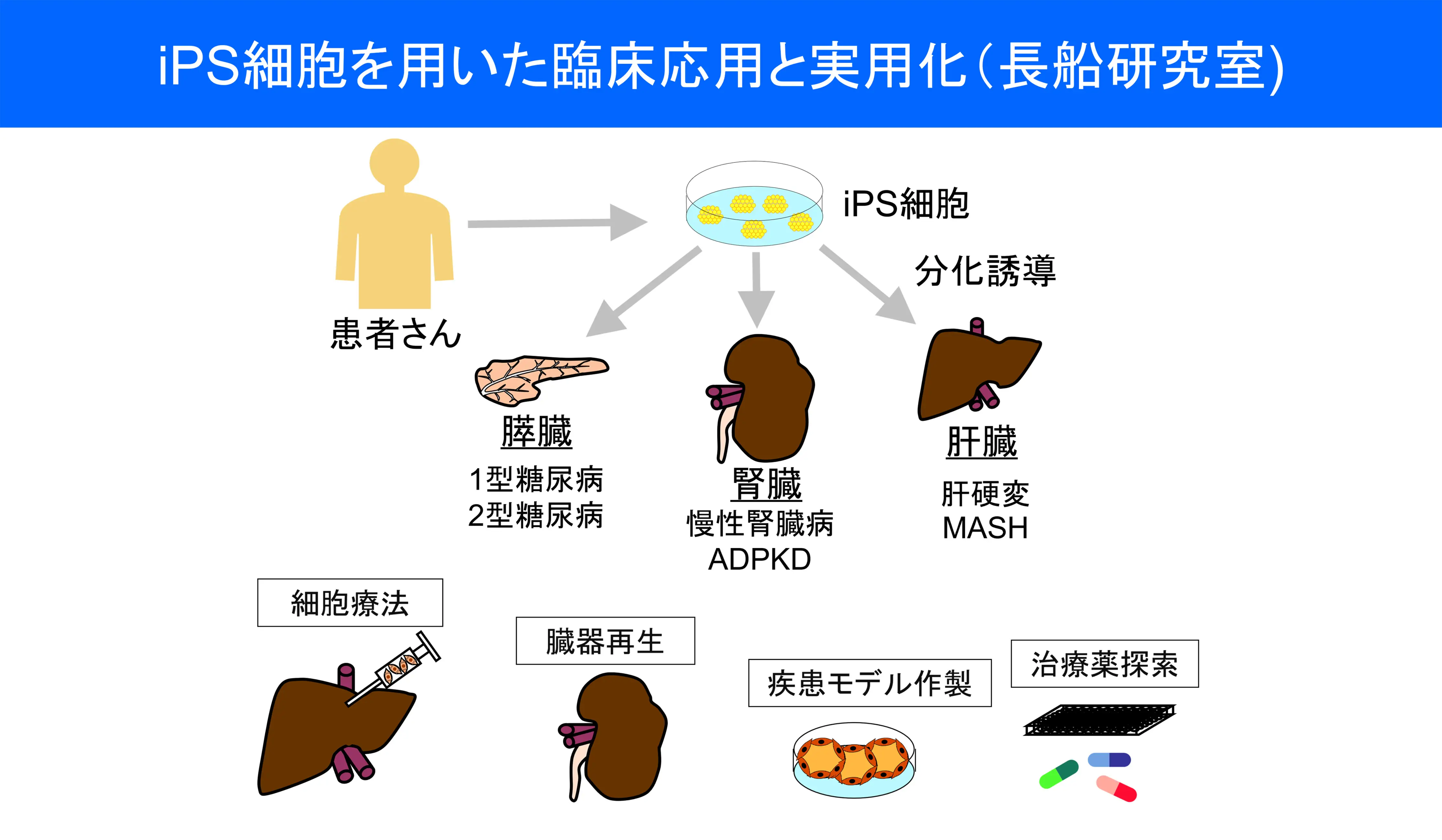 長船先生の研究概要
長船先生の研究概要
「進行を遅らせる」から「進行を止める」治療へ
――現在開発中のiPS細胞を使った腎細胞療法について、具体的なメカニズムを教えてください。
長船先生:私たちが現在進めているのは、iPS細胞から作製した「腎前駆細胞(ネフロン前駆細胞)」という、腎臓の元となる細胞を移植する治療法です。
腎臓は発生過程が非常に複雑で、複数の起源が組み合わさってできるため、再現が最も難しい臓器の一つです。そのうえ、私が研究を始めた当初、神経や心臓などと比較して発生過程の解明が進んでいませんでした。長年の基礎研究でようやくそのプロセスを解き明かし、細胞の作製方法を確立しました。
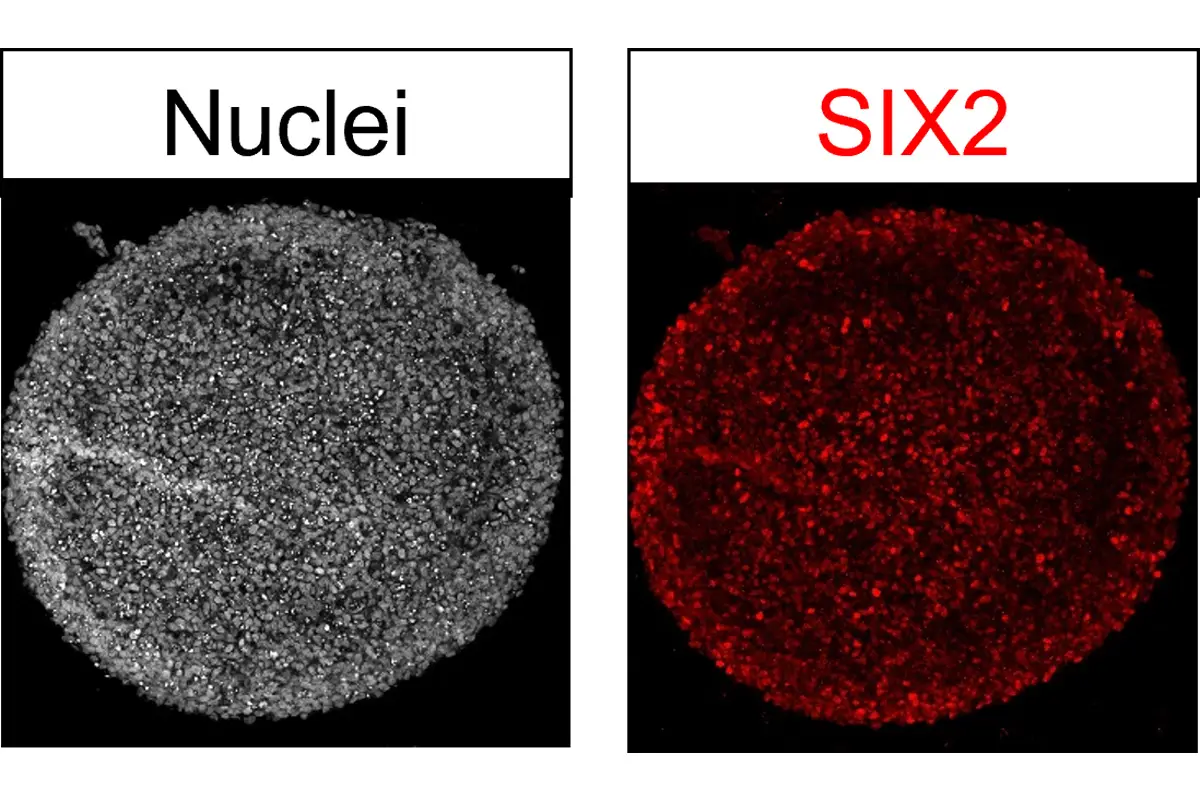 iPS細胞から作製されたネフロン前駆細胞
iPS細胞から作製されたネフロン前駆細胞
――移植された細胞は、体内でどのように働くのでしょうか。
長船先生:第一段階として目指しているのは、移植した細胞から様々な栄養因子を分泌させ、病気で壊れつつある腎臓の細胞死を食い止めることです。これにより、病気の進行を「遅らせる」のではなく、「止める」ことを狙っています。
そして将来的には、移植した細胞が腎臓の組織の一部として組み込まれ、失われた機能を代替する段階を目指しています。これが実現して初めて、腎臓病治療において「機能が良くなる」という状態を目指せるようになります。
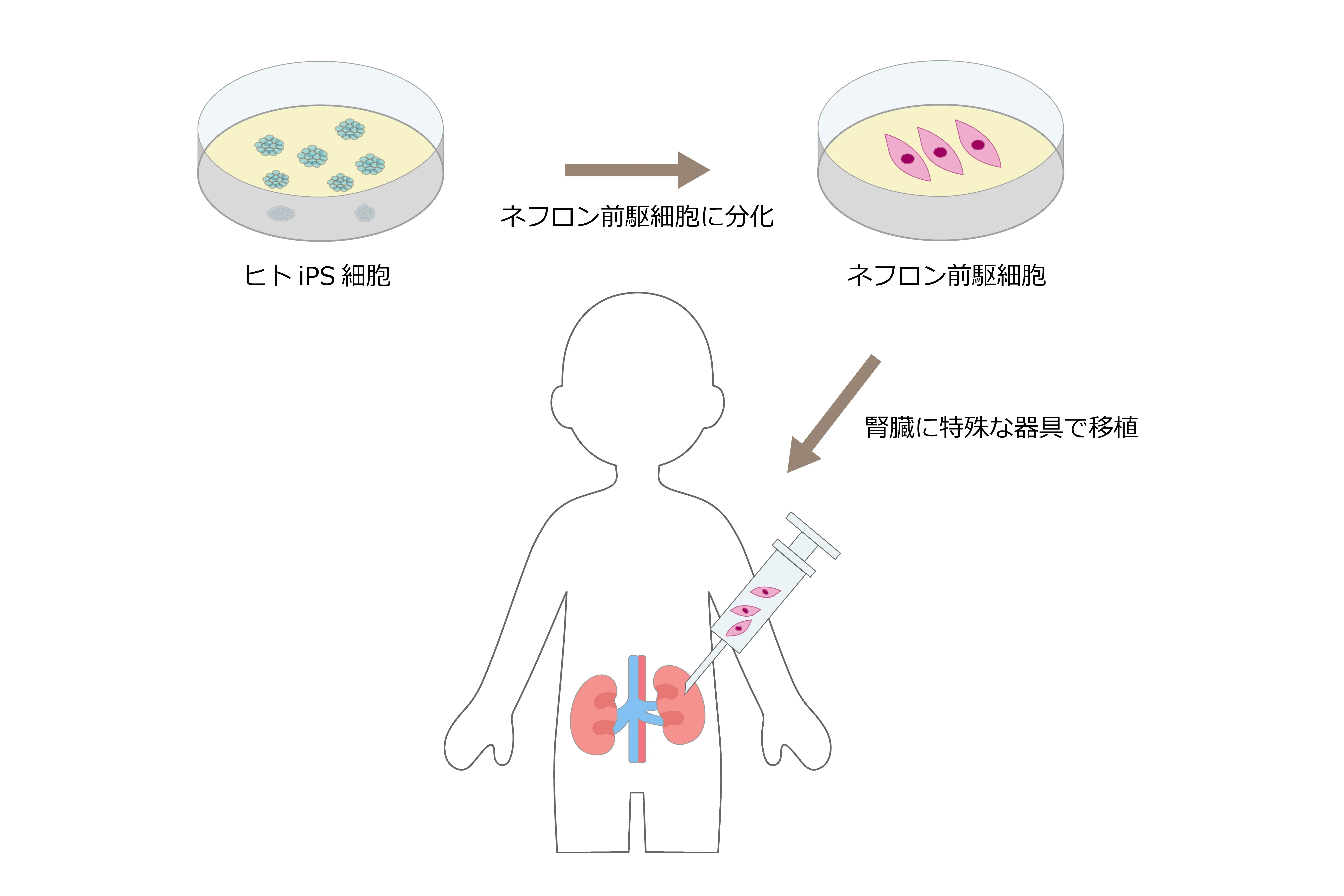 腎細胞療法の仕組み
腎細胞療法の仕組み
――今後のマイルストーンについて教えてください。
長船先生:先ほど申し上げた通り、直近の目標として、2年後に患者さんへの投与(臨床試験)を開始できるよう準備を進めています。基礎研究の段階から、実際に患者さんに届ける「医療」へとフェーズが移行しつつある重要な時期です。ここで必須となるのが、日機装と共同開発している大量培養装置です。
手作業では不可能だった「10億個」の壁
――なぜ、大量培養装置が必須となるのでしょうか。
長船先生:基礎研究で使用するマウスは体重が約30gで、治療には100万個程度の細胞が必要になります。そして人間の体重はその2,000倍以上。人間に十分な治療効果をもたらすためには、患者さん1人あたり約10億個という膨大な数の細胞が必要になるのです。
これを従来の手作業(培養皿による培養)で行おうとすると、患者1人分の細胞を作るのに1万枚以上の培養皿が必要になります。均質に、安全に管理しながらこれだけの培養を手作業で行うことは物理的に不可能です。実用化のためには、自動化・機械化が避けて通れない課題でした。
――培養の自動化・機械化が課題だったのですね。日機装とは、どのような経緯で協業が始まったのでしょうか?
長船先生:2010年、私は米国での学会に参加し、「バイオ人工腎臓」の開発パートナーを探すために、出展していた医療機器メーカー5〜6社に声をかけました。しかし、ほとんどの企業には相手にされず、断られました。その中で唯一話を聞いてくれたのが日機装であり、当初から担当してくれたのが神保さんでした。
日機装 神保:私自身も「バイオ人工腎臓」に関心を持っていたので、声をかけていただいたときは本当に嬉しかったですね。ただ、当時の日機装は医療機器メーカーであり、細胞を扱う設備も知見も全くありませんでした。それでも「一緒にやらないか」と言ってくださった先生の熱意に共感し、社内を説得して金沢製作所に細胞培養室を一から作るところからプロジェクトが始まりました。
 左:日機装 神保部長/右:長船先生
左:日機装 神保部長/右:長船先生
――全くのゼロからのスタートだったのですね。開発はどのように進んだのでしょうか。
長船先生:当初は「バイオ人工腎臓」を目指していましたが、研究過程で細胞そのものを移植する「細胞療法」の有効性が判明しました。さらに、細胞を100倍に増やす技術が開発されたことで、「細胞を大量培養する装置を作る」ことへとシフトしたのです。
細胞は生き物ですから、非常にデリケートで、少しの条件変化で性質が変わったり、目的外細胞※が混ざってしまったりするリスクがあります。とくにiPS細胞由来の製品では、未分化な細胞が残ると腫瘍化のリスクがあるため、均質で安全な細胞だけを安定的に供給する必要があります。
日機装 神保:ここで役立ったのが、日機装が発電所の水質調整装置や透析装置の開発で培ってきた流体制御やセンシング技術です。温度や濃度を厳密に管理し、常に一定の環境を保つ技術は私たちの得意分野です。これらの技術を組み合わせることで、先生が求める厳しい基準をクリアする装置の基本形を作り上げることができました。
長船先生:私が「あっさり作ることができた」と驚くほど、スムーズに装置が形になりましたよね。もちろん、目的外細胞を排除し、均質な細胞を安定供給するための微調整は現在も続いていますが、日機装の技術がなければ、ここまでたどり着くことはできませんでした。
※目的外細胞:人工的に細胞を分化させる際に発生する、未分化の細胞や本来意図していない種類の細胞。
 リジェネフロ社に設置された日機装製 大量培養システム
リジェネフロ社に設置された日機装製 大量培養システム
――今後日機装に期待することを教えてください。
長船先生:培養細胞数のスケールアップを進めながら、現在は腎細胞だけでなく肝細胞でも大量培養の検討を始めています。色々な細胞で日機装の装置が使えるのではないかと期待しています。
「透析のない世界」を目指す、矛盾なき共創
――この自動培養装置が完成した先には、どのような未来が待っているのでしょうか。
長船先生:国内の腎臓病患者数は約2,000万人、世界では8億5,000万人に達すると言われています。自動化システムが確立すれば、一度に大量の細胞を製造でき、コストを下げることが可能です。そうなれば、日本国内だけでなく、世界中の患者さんに治療を届けられるようになります。
実は、私はアメリカに留学していた期間を除いて臨床医としての勤務を続けており、現在も大学病院の腎臓内科外来や月3回程度の透析クリニックでの診療を行っています。
透析患者さんが直面する現実は過酷です。週3回の通院、食事制限、透析後の疲労感、そして急変のリスク。「透析をしなくて済むようにしたい」「進行を食い止めたい」という思いは、臨床の現場に立つたびに強くなります。
――透析事業を展開する日機装と、「透析をしなくて済む治療」を目指すリジェネフロ。一見すると相反するようにも見えます。
長船先生:確かに、日機装の主力事業の一つは透析装置ですから、私との共同研究は矛盾するように見えるかもしれません。しかし、私たち両者は「患者さんの苦しみを取り除く」という最上位の目的で深く結びついています。
日機装 神保:おっしゃる通りです。透析医療と細胞培養、いずれのアプローチであっても、自分たちの持てる技術でより良い医療に貢献したいという日機装の想いは、先生と同じです。引き続き透析事業を展開し、透析を必要とする患者さんのQOL向上に寄与しながら、先生が目指す腎細胞療法の実現に向けて、これからも連携していきます。
長船先生:現在の透析患者さんにはより良い透析医療を、そして未来の患者さんには透析に至らない新たな治療法を。アプローチは違えど、見据えている未来は同じです。

<iPS細胞研究基金について>
これまでにiPS細胞研究は大きく発展してきましたが、医療として確立されるまでにはまだまだ時間がかかります。この長い道のりを走り続けるための財源として、多くの方々からのご寄付で成り立っている「iPS細胞研究基金」は、研究活動を支える重要な柱となっています。
今は不可能な治療を一日も早く可能にするために、iPS細胞研究基金へのご支援をお願いいたします。
iPS細胞研究基金へのご支援についてはこちら。







